විද්යාඥයන් සහ වෛද්යවරුන්ගෙන් සැදුම්ලත් කණ්ඩායමක් විසින් යුරෝපීය ඖෂධ ඒජන්සිය වෙත විවෘත ලිපියක් යොමුකරමින් එය විසින් අනුමත කරන ලද කොරෝනා එන්නත් වර්ග පිළිබඳවල සෞඛ්යාරක්ෂිත බවට අදාළව ප්රශ්න ගණනාවක් යොමු කර තිබේ. එම ප්රශ්නවලට පිළිතුරු දිය නොහැකි නම් අදාළ එන්නත් සඳහා එය විසින් ලබාදුන් අනුමැති ඉවත් කරගන්නා ලෙසද ඔවුහු ඉල්ලා සිටිති. එම ලිපියට දින හතක් ඇතුළත ප්රතිචාර දක්වන ලෙස ඔවුහු ඉල්ලා සිටියහ.
දැනට COVID-19 වසංගතයට එරෙහිව විවිධ සමාගම් ගණනාවක් සිය වැක්සීන ජාත්යන්තර ඖෂධ වෙළඳපොළට ඉදිරිපත් කර තිබේ.
මේවා නම්, BioNTech, Fosun Pharma, Pfizer යන සමාගම් ඒකාබද්ධව නිෂ්පාදනය කරන ලද Comirnaty, Moderna Biotech සමාගම විසින් නිපදවන ලද Covid-19 Vaccine Moderna, AstraZeneca සමාගම විසින් නිපදවන ලද AstraZeneca/Covid-19 (පසුව මෙහි නම Vaxzevria නමින් වෙනස් කරනු ලැබිණි.), Janssen-Cilag/Johnson und Johnson සමාගම් විසින් නිපදවන ලද Covid-19 Vaccine Janssen, රුසියාවේ ගම්ලයා සමාගමේ ලද Sputnik V, චීනයේ Sinovac, AstraZeneca සමාගම සහ ඉන්දියාවේ පූනේ හි Serum Institute of India (SII) සමාගම ඒකාබද්ධව නිෂ්පාදනය කරන Covishield, ආදිය වේ.
මෙයින් Comirnaty සහ Moderna වැක්සීන පදනම්වී ඇත්තේ මෙසෙන්ජර් රයිබෝනියුක්ලික් අම්ල නැතහොත් mRNA තාක්ෂණය මතයි. මෙම තාක්ෂණය මෙවැනි වසංගතයක් සඳහා භාවිතාවන්නේ පළමුවරටය. නිෂ්පාදකයන්ට අනුව මෙම වැක්සීන තාක්ෂණයට අයත් වැක්සීන ක්රියාත්මක වන්නේ මෙලෙසය.
“Comirnaty වැක්සීනය විසින් COVID-19 වෛරසයයට මුහුණ දීමට ශරීරය සුදානම් කෙරේ. SARS-CoV-2 වෛරස සෛල තුළට ඇතුළු වීමට යොදාගන්නා ස්පයික් ප්රෝටීනය සෛලය තුළ නිපදවන ලෙස වැක්සීනයේ අඩංගු mRNA මොලිකියුලවලට උපදෙස් ලබා දී තිබේ. යම් පුද්ගලයෙකුට වැක්සීනය එන්නත් කළ පසුව ඔහුගේ හෝ ඇයගේ සමහර සෛල ඉහත mRNA මොලිකියුල මත ඇති පණිවිඩය කියවා ඒ අනුව වෛරසයේ ස්පයික් ප්රෝටීනය තාවකාලිකව නිපදවයි. එවිට පුද්ගලයාගේ ප්රතිශක්ති පද්ධතිය විසින් මෙම ස්පයික් ප්රෝටීනය බාහිර ද්රව්යයක් ලෙස හඳුනා ගෙන එය විනාශ කිරීම සඳහා T සෛල හෙවත් සුදු රුධිර සෛල සක්රිය කරයි. පසුව එම පුද්ගලයාගේ ශරීරය තුළට SARS-CoV-2 වෛරසය ඇතුළු වූ අවස්ථාවක ඔහුගේ ප්රතිශක්තිය පද්ධතිය විසින් එය හඳුනාගෙන එයට එරෙහිව ශරීරය ආරක්ෂා කරයි. වැක්සීනයේ අඩංගු mRNA ශරීරය තුළ රඳා නොපවතින අතර එන්නත් කිරීමෙන් කෙටි කාලයකට පසුව එය විසංයෝජනය වේ.“

මහාචාර්ය සුචරිත් බාක්දි
AstraZeneca/ Vaxzevria ඇතුළු ඉහත සඳහන් සෙසු සියලු වැක්සීන වර්ග අයත් වෙනුයේ Live-attenuated vaccines ගොනුවටය. එමගින් සිදු කරනුයේ වෙන්කරගත් වෛරසය විද්යාගාරය තුළ දී දුර්වල කර එය ශරීරයට එන්නත් කිරීම ය. බොහෝ සම්ප්රදායික වැක්සීන මේ ගොනුවට අයත් වේ. සෛද්ධාන්තිකව ගත් කළ දුර්වල කරන ලද වෛරසය මිනිස් සිරුර තුළ ප්රතිනිෂ්පාදනය වීමට ඉඩක් නැත. ප්රතිශක්ති පද්ධතිය විසින් අදාළ වෛරසය හඳුනාගත් පසුව එයට එරෙහිව ප්රතිදේහ නිපදවමින් ශරීරය ආරක්ෂා කරයි.දැනට යුරෝපා සංගමය තුළ භාවිතය සඳහා රුසියාවේ Sputnik V සහ චීනයේ Sinovac යන වැක්සීන් දෙකට හැරෙන්නට ඉහත සඳහන් අන් සියලු වැක්සීන් වර්ගවලට යුරෝපීය ඖෂධ ඒජන්සිය විසින් හදිසි තත්ත්වයන්හිදී භාවිතා කරන රෙගුලාසි යටතේ එනම් ආවස්ථික අලෙවි අනුමැතිය (Conditional Marketing Authorisation) යටතේ අනුමැතිය දී ඇත.
ශ්රී ලංකාවේ භාවිතයට ගනු ලබන්නේ Oxford- Astra zeneca සමාගම සහ ඉන්දියාවේ පූනේ හි Serum Institute of India (SII) සමාගම ඒකාබද්ධව නිෂ්පාදනය කරන Covishield නම් වැක්සීනයයි. එය ලෝක සෞඛ්ය සංවිධානය විසින් පවත්වාගෙන යනු ලබන COVAX බෙදාහැරීමේ ව්යාපෘතිය යටතේ ශ්රි ලංකාවට ලබා දී තිබේ.
මහාචාර්ය සුචරිත් බාක්දි ඇතුළු ඉහත වෛද්යවරුන් එම ලියා යවා ඇත්තේ 2021 පෙබරවාරි 28 වැනි දිනය. දින සතක් ඇතුළත එම ලිපියට ප්රතිචාර දක්වන ලෙස ඔවුහු ඉල්ලා සිටිය ද මාර්තු 26 වැනි දා තෙක්ම එයට කිසිදු ප්රතිචාරයක් ලැබී නොතිබිණි. මසකට ආසන්න කාලයකට පසුව යුරෝපීය ඖෂධ ඒජන්සියට එම ලිපියට පිළිතුරක් ලිවීමට බල පෑ වෙනත් බරපතල තත්ත්වයක් උද්ගත වෙමින් තිබූ බව පැහැදිලි ය. එනම් යුරෝපයේ රටවල් ගණනාවක් විසින් Astra zeneca සමාගමේ වැක්සීනය භාවිතය අත්හිටු වීමය. 2021 මාර්තු 16 වැනි දින යුරෝපයේ රටවල් කීපයක් වන එස්තෝනියාව, ලිතුවේනියාව, සහ ලක්සම්බර්ග් විසින් Astra zeneca එන්නත භාවිතය අත්හිටුවන ලදි. ඒ ලේ කැටිගැසීම් ඇතුළු දරුණු ආබාධ රාශියකට එන්නත් ගත්තවුන් ලක්වීම සහ ඇතැමුන් මරණයට පත්වීම නිසාය. අනතුරුව ස්වීඩනය, ලැට්වියාව, නෙදර්ලන්තය, ඩෙන්මාර්ක්, ප්රංශය, ඉතාලිය, ස්පාඤ්ඤය සහ ජර්මනිය විසින්ද මෙම එන්නත භාවිතය අත්හිටුවන ලදි. එසේ වුවද එයට අනුමැතිය ලබා දුන් යුරෝපීය ඖෂධ ඒජන්සිය මේ තත්ත්වය පිළිබඳ කිසිවක් ප්රකාශ කිරීමට ඉදිරිපත් වූයේ නැත.
සැබැවින්ම මහාචාර්ය සුචරිත් බාක්දි ඇතුළු පිරිස මතුකර තිබූ එක් වැදගත් ප්රශ්නයක් නම් Astra zeneca වැක්සීනය එන්නත් කරනු පුද්ගලයන් රැසකට ලේ කැටි ගැසීම ඇතුළු ඉතා හානිකර ආබාධයන්ට මුහුණ දීමට සිදුවීමයි. ඉන් සමහරෙකු මරණයට පත් වී තිබිණි. මෙම වැක්සීනය භාවිතය අත් හිටු වූ රටවල් එය සිදු කළේද ඇතැම් පුද්ගලයන් ලේ කැටි ගැසීමේ අක්රමිකතා හේතුවෙන් මරණයට පත් වීම නිසාය. මෙම රටවල වෛද්යවරුන් සහ මහජනයා වෙතින් එල්ල වූ බලපෑම් හේතුවෙන් ඒවායේ ආණ්ඩු විසින් යුරෝපීය ඖෂධ ඒජන්සියට යම් බලපෑමක් එල්ලවන්නට ඇත. අවසානයේ මෙම ලිපියට මාර්තු 26 වැනි දින පිළිතුරු සපයන්නට ඔවුන් තීරණය කරන්නට ඇත්තේ ඒ නිසා වන්නට ඇත.
ඔවුහු දින කීපයකට පසුව, ඉහත රුධිර කැටිගැසීම් හා සම්බන්ධ සිදුවීම් හා වැක්සීන අතර සම්බන්ධයක් තහවුරු කිරීමට සාක්ෂි නැතැයිද, මෙම එන්නත භාවිතයෙන් ලැබෙන ප්රයෝජන ඉන් සිදුවන හානියට වැඩි යයි ද පවසමින් දිගටම වැක්සීනය භාවිතයට ගැනීම නිර්දේශ කළෝය. ලෝක සෞඛ්ය සංවිධානයද එම ප්රකාශයම පුනරුච්ඡාරණය කරමින් වැක්සීනය තවදුරටත් අනුමත කරන ලදි. මේ අනුව කලින් මෙම වැක්සීනය භාවිතය අත්හිටුවන ලද රටවල් කීපයක් හැරෙන්නට සෙසු සියලු රටවල් එකින් එක යළිත් වැක්සීනය භාවිතය පටන් ගන්නා ලදි. ඉන් දින කීපයකට පසුව කැනඩාව විසින් වයස 55ට අඩු පුද්ගලයන් හට Astra zeneca වැක්සීනය දීම අත්හිටුවන ලදි. ඒ අසාමාන්ය ලෙස රුධිරයේ ලේ කැටිගැසීම් පිළිබඳ සිදුවීම් වාර්තා වීමත් සමගමය. ඉන් අනතුරුව ජර්මනිය යළිත් වයස 60 ට අඩු පුද්ගලයන් වෙත එන්නත් ලබාදීම අත්හිටුවන ලද්දේ එම හේතුවම දක්වමිනි. වැක්සීන ගැනීමෙන් පසුව සිදු වූ රුධිර කැටිගැසීම් නිසා සිදුවූ මරණ ගණනාවකට පසුව බ්රිතාන්ය විසින් Astra zeneca වැක්සීනය සහ ඒ මරණ අතර සම්බන්ධයක් ඇතැයි පිළිගෙන තිබේ.
යුරෝපීය ඖෂධ ඒජන්සිය ඒ ගැන තවදුරටත් පරීක්ෂණ පවත්වමින් සිටින බව පවසයි.
මේ අතර ඉන්දියාවේද Covishield එන්නත ලබාගත් පුද්ගලයන් ගණනාවක් මරණයට පත්වීම් සහ රෝහල්ගතවීම් පිළිබඳවාර්තා වී තිබේ.
මහාචාර්ය සුචරිත් බාක්දි ඇතුළු විශේෂඥයන් යුරෝපීය ඖෂධ ඒජන්සියේ වෙත යොමු කරන ලද ලිපියේ මෙසේ සඳහන් වේ.
“…COVID-19 සඳහා භාවිතයට මුදා හැර ඇති ජාන මූලික එන්නත් ලබාගැනීමෙන් පසුව නිරෝගී සෞඛ්ය සම්පන්න තරුණ පුද්ගලයන් ගණනාවක් ඉතා දරුණු අතුරු ආබාධවලට ගොදුරු වීම පිළිබඳව ඇති වාර්තා කෙරෙහි අපි අවධානය යොමු කරමු. එමෙන්ම මීට අමතරව ලෝකය පුරා වැඩිහිටි නිවාසවල සිටින්නවුන්හට COVID-19 එන්නත් ලබාදීමෙන් පසුව ඇති වූ ඛේදජනක තත්ත්වය පිළිබඳව පළ වූ විවිධ මාධ්යයන් විසින් වාර්තා කර තිබිණි. මෙම සෑම පුද්ගලයෙකුටම මුහුණපෑමට සිදු වූ තත්ත්වයන් අවාසනාවන්ත අහම්බයන් වන්නට ඇති ඉඩකඩ අප විසින් පිළිගනු ලබන අතරම මෙම රෝගී තත්ත්වයන් සහ මරණවලට බලපෑ හේතූ සොයාබැලීමට දැඩි විමර්ශනයක් මේ දක්වා සිදු නොවීමද පශ්චාත් මරණ පරීක්ෂණ නොපැවැත්වීමද මෙහිදී අප විසින් සැළකිල්ලට ගෙන තිබේ.
යුරෝපීය ඖෂධ ඒජන්සිය European Medicines Agency (EMA) විසින් මෙම එන්නත් භාවිතය සඳහා අවසර දීමට පෙර මෙම එන්නත්වල සුරක්ෂිතතාව පිළිබඳව සොයා බැලිය යුතු මූලික කරුණු ප්රමාණවත් පරිදි පරීක්ෂාවට ලක්කරනු ලැබ ඇත්දැයි අපි වඩාත් නිශ්චිතව ප්රශ්න කරමු…“
මෙම සියලු COVID-19 වැක්සීන ශරීර ගත කිරීමකින් පසුව ශරීරය තුළ සිදුවන එහි ක්රියාකාරිත්වය නිසා එක් එක් අදියරේදී මතු එය විසින් මතු කළ හැකි විය අවදානම් සහගත තත්ත්වයන් පිළිබඳව සෛද්ධාන්තික කරුණු ඉදිරිපත් කරන මහාචාර්ය බාක්දි ඇතුළු පිරිස, ඒ ඒ අදියර පිළිබඳව සත්වයන් යොදා කරන ලද පරීක්ෂණ වලදී එවන් අවදානම් සහගත තත්ත්වයක් මතුවීමට ඇති ඉඩ කඩ බැහැර කිරීමට යුරෝපීය ඖෂධ ඒජන්සිය සමත්ව ඇත්දැයි ප්රශ්න කරති.
ඔවුහු සිය පළමු ප්රශ්නය තුළ වැක්සීනයේ අන්තර්ගතය රුධිර ප්රවාහයට එක් වී සමස්ත ශරීරය පුරා පැතිරයාමට ඇති අවදානම ගැනප්රශ්න කරති.
“මෙම අන්තහ් පේශීය එන්නත intramuscular injection ලබා දුන් පසුව මෙම ජාන ප්රතිකාරක වැක්සීනය රුධිර ප්රවාහයට එක් වී ශරීරය පුරා පැතිර යාමට ඇති ඉඩකඩ අපේක්ෂා කළ යුත්තකි. පූර්ව සායනික සත්ව පරීක්ෂණ වලදී pre-clinical animal models මෙම ශක්යතාව බැහැර කර ඇති බවට යුරෝපීය ඖෂධ ඒජන්සිය (EMA) විසින් මෙම වැක්සීන් වර්ග තුන මනුෂ්යයන් සඳහා භාවිතය අනුමැතිය දීමට පෙර තහවුරු කරගැනීමට සමත් වූයේ නම් ඊට අදාළව එය සතු පරීක්ෂණාත්මක සාක්ෂි ඉදිරිපත් කරන ලෙස අපි ඉල්ලා සිටිමු.“
එයට යුරෝපා ඖෂධ ඒජන්සියේ පිළිතුර මෙසේය,
“වැක්සීනයේ අඩංගු mRNA අවශෝෂණය ප්රධාන වශයෙන්ම දැකිය හැකි වන්නේ එන්නත ශරීරගත කල ස්ථානය ආශ්රිතව ප්රතිශක්ති පද්ධතියට අයත් භක්ෂාණු (macrophages) සහ ද්රැමක (dendritic) සෛලවල සහ වසා ගණ්ඨ තුළය. මෙයට අමතරව ප්ලාස්මාවේ සහ අනෙකුත් පටක වල දින 9ක් පමණ කාලයක් mRNA දැකිය හැකි විය. දැනට පවතින COVID-19 mRNA වැක්සීන භාවිතයේදී මතුවිය හැකි සෞඛ්ය ගැටළු හඳුනාගැනීම සඳහා මනුෂ්යයන් වෙත ලබා දෙන මාත්රාවට සාපේක්ෂව ඉහළ වැක්සීන මාත්රාවන් යොදා ගනිමින් සතුන් සම්බන්ධව කරන ලද පරීක්ෂණවලදී මෙම තත්ත්වය අධ්යයනය කරන ලදි. මෙහිදී දැකිය හැකි වූයේ ලිපිඩ නැනෝ අංශු තුළ සංයෝජනය කරන ලද වැක්සීනයේ mRNA ප්රධාන වශයෙන්ම ශේෂ වනුයේ එන්නත ලබාදුන් ස්ථානයේ බවය. එයට අමතරව ඉතා සුළු ප්රමාණයක් අක්මාව වැනි අනෙකුත් පටක කරා ගමන් කළ හැකිය.
COVID-19 AstraZeneca වැක්සීනය සම්බන්ධයෙන් එම වාහකයම (vector) සහ වෙනත් වෛරස් ප්රෝටීනයක් යොදාගනිමින් කරන ලද පරීක්ෂණවලදී දැකිය හැකි වූයේ එන්නත් කරන ලද වෛරස් වාහකය ශේෂ වනුයේ එන්නත ලබාදුන් ස්ථානයේ බවය. ඉතා සුළු ප්රමාණයක් පමණක් සෙසු පටකවල නිරීක්ෂණය කළ හැකි විය.
වැක්සීන් වර්ග තුනට අදාළව පරීක්ෂණාගාර තත්ත්වයන් තුළ සත්වයන් යොදාගනිමින් සිදු කරන ලද සායනික නොවන අධ්යයනයන් වලදී පටක තුළට ඒවා පැතිරීම හා සම්බන්ධිතව කිසිදු සෞඛ්යමය අවදානමක් හඳුනා ගැනීමට නොහැකි විය.”
මෙහිදී යුරෝපා ඖෂධ ඒජන්සිය විසින් වැක්සීනයේ අන්තර්ගතය රුධිර ප්රවාහයට එක්වන බවට වක්රව පිළිගනිමින් බාක්දි ඇතුළු පිරිසගේ උපකල්පනය නිවැරදි බව තහවුරු කර තිබේ. වැක්සීනයේ අනත්ර්ගතය රුධිර ප්රවාහයට එක් නොවන්නේ නම් එය අක්මාව හෝ අනෙකුත් පටක කරා ගමන් නොකරනු ඇත. එම පටක තුළ වැක්සීනයේ අන්තර්ගතයන් දක්නට ලැබීම ඔවුහු සාධාරණීකරණය කරනුයේ සතුන්ට ලබා දුන් මාත්රාව මිනිසුන්ට ලබා දෙන මාත්රාවට වඩා ඉතා ඉහළ අගයක් ගන්නා බව පැවසීම මගිනි.“ සෞඛ්ය අවදානම් හඳුනාගැනීම“ රඳා පවතිනුයේ පර්යේෂකයන් සහ විශ්ලේෂකයන් ඒවාට දෙන අර්ථකතන අනුවය. එම අර්ථකතන රඳා පවතිනුයේ ඔවුන්ගේ අවශ්යතාවන් සහ ප්රමුඛතාවන් මතය.
මීළඟ ප්රශ්නය වන්නේ වැක්සීනය රුධිර ප්රවාහයට එක්වන්නේ නම් ඒවා රුධිර නාලවල අභ්යන්තර පටකයේ සෛල තුළට අවශෝෂණය වන්නේ ද යන්න පිළිබඳවය. එම ප්රශ්නයට පිළිතුර ලෙස යුරෝපා ඖෂධ ඒජන්සිය ප්රකාශ කරනුයේ වැක්සීනයේ වාහකය (vector) හෝ ප්රතිග්රාහකය (receptor) රුධිරනාල අභ්යන්තර පටක සෛල තුළට අවශෝෂණය වන බවට ද එහි ප්රතිග්රාහකය විසින් අදාළ පටක සෛල තුළ ජාන ප්රකාශන ක්රියාවලිය සිදු කරන බවටද කිසිදු සාක්ෂියක් නැති බවය. එසේ පවසන අතරම එයට පරස්පරව යන ප්රකාශයක් මගින්, එය සිදුවන්නේ නම් ඒ “ ඉතා සුළු ප්රමාණයකින් “ සිදුවීමට “ඉඩ ඇති“ දෙයක් බව ද පිළිගනී. මෙහි ඇත්තේ අවදානම අවප්රමාණ කිරීමේ උත්සාහයකි. mRNA වැනි ජානමය මොලිකියුල වල බලපෑම් ආරම්භ වීමට “ඉතා සුළු “ප්රමාණයක් ආරම්භයේදී ප්රමාණවත්ය. එම වැක්සීන වල ප්රතික්රියාවන් සියල්ල අපේක්ෂිත ඒවා බවද අනපේක්ෂිත ප්රතික්රියාවන්ගේ අවදානම සායනිකව කළමණාකරණය කරගත හැකි මට්ටමක පවතින බවද එම පිළිතුරේ වැඩිදුරටත් සඳහන්වේ. එහි දී මතුවන ගැටළුව මෙයයි. දසදහස් සංඛ්යාත නැතහොත් මිලියන සංඛ්යාත ජනකායකට දෛනිකව මේ එන්නත් ලබා දෙන විට එකී අවදානම් සහගත අනපේක්ෂිත ප්රතික්රියාවන් කල්තබා හඳුනාගැනීමට අවශ්ය පසුවිපරම් ක්රියාවලියක් පවත්වාගෙන යාමට යාන්ත්රණයක් හෝ ඊට හැකියාවක් යුරෝපයේ හෝ ලෝකයේ කිසිදු රටක පවතින්නේ ද යන්නය. සාමාන්ය ජනයා සඳහා වන විවෘත භාවිතයේදී පළමු සහ දෙවන එන්නත් වාර අතර හෝ දෙවන එන්නත් වාරයෙන් පසුව, අදාළ ගැටළු හඳුනාගැනීම සඳහා කී දෙනෙකුගේ රුධිර පරීක්ෂාවන් සිදු කර ඇත් ද? එවැන්නක් සිදු නොකර එකී අවදානම් සහගත තත්ත්වයන් “සායනිකව කළමණාකරණය“ කරගත හැක්කේ කෙසේද? (මෙම සම්පූර්ණ ප්රශ්නය සහ පිලිතුර සඳහා මෙම සබඳතාවට පිවිසෙන්න)

එමර් කුක්
මීළඟ ප්රශ්නය වනුයේ ඊට කලින් වෙනත් වෛරස් වලින් සිදු වූ ආසාදනවලට ප්රතිචාරයක් ලෙස නිර්මාණය වූ සුදු රුධිරාණු, වැක්සීනයේ අඩංගු mRNA විසින් ඊට දී ඇති උපදෙස් අනුව නිපදවන වෛරස් ස්පයික් ප්රෝටීන සහිත සෛලවලටපහර දීමට ඉඩක් ඇත්දැයි යන්නයි.“…වැක්සීනයේ ජාන ප්රකාශන (gene expression) ක්රියාවලියේදී එහි ස්පයික් ප්රෝටීන විසින් නිපදවන නියුක්ලික් අම්ල සහ පෙප්ටයිඩ MHC I පථය හරහා සෛලයේ මධ්ය කුහර පෘෂ්ඨය වෙත ගමන් කරනු ඇති බවට අපේක්ෂා කළ හැකිය. බොහෝ නිරෝගී මිනිසුන් තුළ පවතින CD8 ලිම්පොසයිට (lymphocytes) වලට මෙවැනි පෙප්ටයිඩ හඳුනාගැනීමේ හැකියාවක් පවතී. ඒ COVID ආසාදනයට පෙර වෙනත් වර්ගවල කොරෝනා වෛරසවලට දක්වන ලද ප්රතිචාර නිසා විය හැකිය. එනිසා මෙම ලිම්පොසයිට සුදු රුධිරාණු විසින් අදාළ සෛලවලට (වැක්සීනය විසින් නිෂ්පාදිත ස්පයික් ප්රෝටීන සහිත සෛලවලට) පහර දීමට ඇති ඉඩකඩ අප විසින් අනුමාන කළ යුතුය. පූර්ව සායනික සත්ව පරීක්ෂණ වලදී pre-clinical animal models මෙම ශක්යතාව බැහැර කර ඇති බවට යුරෝපීය ඖෂධ ඒජන්සිය (EMA) විසින් මෙම වැක්සීන් වර්ග තුන මනුෂ්යයන් සඳහා භාවිතය අනුමැතිය දීමට පෙර තහවුරු කරගැනීමට සමත් වූයේ නම් ඊට අදාළව එය සතු පරීක්ෂණාත්මක සාක්ෂි ඉදිරිපත් කරන ලෙස අපි ඉල්ලා සිටිමු.“
මෙම ප්රශ්නයට ප්රතිචාර ලෙස යුරෝපීය ඖෂධ ඒජන්සිය එවැනි අවදානම් සහගත තත්ත්වයක් සඳහා එනම්, ප්රතිශක්තිමය විෂවීමක් හෝ ස්වයං ප්රතිශක්තිකත්වය (autoimmunity)ක් හෝ වැක්සීන්- ප්රේරිත බහුලීකරණය (vaccine-induced enhancement of disease – VAED) ක් සම්බන්ධව කිසිදු සාක්ෂියක් සතුන් හෝ මිනිසුන් සම්බන්ධයෙන් කරන ලද කිසිදු පරීක්ෂණයකින් හමු වී නැති බව සඳහන් කරයි. (මෙම සම්පූර්ණ ප්රශ්නය සහ පිලිතුර සඳහා මෙම සබඳතාවට පිවිසෙන්න)
මහාචාර්ය බාක්දි ඇතුළු පිරිසගේ ලිපියේ 4,5,6,7 වැනි ප්රශ්නවලින් ඔවුහු පිළිවෙළින් අවධානය යොමු කරනුයේ “..රුධිරනාලවල වලට සිදුවන හානියේ ප්රතිඵලයක් ලෙස රුධිර පට්ටිකා ක්රියාත්මක වීමෙන් ශරීරය පුරාම ලේ කැටිගැසීමේ තත්ත්වයක් මතුවීමට ඇති ඉඩකඩ..“ වෙත සහ “..රුධිර පට්ටිකා සංඛ්යාව පහත වැටීම, රුධිරය තුළ D-dimer ප්රෝටීනමය තන්තු දක්නට ලැබීම සහ සිරුර පුරා මොළය කොඳු නාරටිය සහ හදවත ඇතුළු අභ්යන්තර අවයවවල පටකවලට හානි සිදුවීම, මෙම අභිනව ව්යාප්තික අන්තහ්වාහිණී රුධිර කැටිගැසීම DIC-syndrome-Disseminated intravascular coagulation තුල මතුවිය හැකි ලේ වහනය වීම්, අධික රුධිරවහනය, මෂ්තිෂ්ක රුධිරවහනය ආදිය සිදුවීමට ඇති ඉඩකඩ..“ පිළිබඳවය.
මෙයට පිළිතුරු ලෙස යුරෝපීය ඖෂධ ඒජන්සිය මෙසේ පවසයි.
“..Moderna COVID-19 වැක්සීනය සඳහා කරන ලද සායනික නොවන අධ්යයනයන්හිදී පයිබ්රිනෝජන් සහ PTT (partial thromboplastin time) අගයන් ඉහළ යාම ඇතුළු රුධිර කැටිගැසීම කෙරෙහි මඳ බලපෑම් දක්නට හැකිවිය. නමුත් Comirnaty වැක්සීනයේදී එය සිදු නොවීය. හැම්ස්ටර් මීයන් යොදා ගනිමින් Comirnaty වැක්සීනයට අදාළව සිදු කරන ලද අධ්යයන වලදී අඛණ්ඩ ලෙස එන්නත් කිරීම්වලට පසුව රුධිර පට්ටිකා අනුපාතය පහත වැටීමක් දැකගත හැකි විය. නමුත් සුළු වශයෙනි. ප්රදාහයික රුධිර පට්ටිකා සක්රියකරණය (inflammation-related platelet activation) සහ “ රුධිර පට්ටිකා භක්ෂණය“ ආදිය හා එහි සම්බන්ධයක් තිබීමට ඉඩ තිබේ. නමුත් රක්තපාතස්ථිතියේ (haemostasis) විපර්යාසයන් හා එහි සම්බන්ධයක් නැත. මේ සියළු වෙනස්වීම් සතුන් වෙත වැක්සීනයේ ඉහළ මාත්රාවන් ලබා දීම මගින් වැඩිකරන ලද ප්රදාහයික- ප්රතිශක්ති ප්රතිචාරයන් හා ගැලපෙයි. එය දින කීපයකට පසුව නැවත යථා තත්ත්වයට පත්විය. මෙම තත්ත්වයන් මනුෂ්යයන්ට අදාළ වීමට ඉඩක් නැත්තේ ඔවුන් වෙත සුළු මාත්රාවන් ලබා දීම නිසාය.
රුධිර පට්ටිකා හා ලේ කැටීගැසීම පිළිබඳ කිසිදු වෙනසක් AstraZeneca වැක්සීනය සතුන්ට ලබා දුන් විට නිරීක්ෂණය කළ නොහැකි විය…”
“..Moderna COVID-19 වැක්සීනයට අදාළව, පුද්ගලයන් කීප දෙනෙකු තුළ අක්මා එන්සයිමවල නැවත යථාතත්ත්වයට පත්කළ හැකි සුළු වෙනස්කම් කීපයක් හැරෙන්නට සායනික රුධිර විද්යාත්මක සහ රසායනික විද්යාත්මක ඇගයීම් තුළ වෙනත් නිශ්චිත රටාවන් දිස් නොවිණි.
Comirnaty වැක්සීනයට අදාළව, සමහර පුද්ගලයන් තුළ ලිම්පොසයිට අනුපාතයේ තාවකාලික පහත වැටීමක් හැර වෙනත් කිසිදු අසාමාන්ය විද්යාගාර ප්රතිඵලයක් අවධි 1 අධ්යයනවලදී වාර්තා නොවීය.
AstraZeneca වැක්සීනයට අදාළ විද්යාගාර ප්රතිඵල සාමාන්ය සායනික සීමාවේ පැවැති අතර එහි ආරක්ෂා සහිත බව ගැන කිසිදු ගැටළුවක් මතු නොවිණි…“
මෙම ප්රශ්නවලට අදාළව යුරෝපීය ඖෂධ ඒජන්සිය පවසන්නේ සායනික සහ සායනික නොවන පරීක්ෂණවලදී ඉහතකී තත්ත්වයන් ගැන කිසිදු සාක්ෂියක් හමු නොවූ බවයි. නමුත් ඊළඟට ඔවුන් පවසනුයේ වැක්සීන පොදු මහජන භාවිතය සඳහා අනුමත කර එය මුදා හැරිය පසුව මාර්තු 16 සහ 18 තදාසන්න කාලයේදී ඉහත වැක්සීන් ලබාගත් ඇතැමුන්ගේ රුධිර පට්ටිකා අනුපාතය පහත වැටීම, රුධිරය කැටිගැසීම අඩුවීම, රුධිර කැටිති ඇතිවීම ආදි ලක්ෂණ මතුවීම පිලිබඳව වාර්තා වීම් සිදු වූ බවයි. එම සිදුවීම් ගැන විමර්ශනයන් ආරම්භ කර ඇති බවත් එහි සඳහන්ය. එමෙන් ම එය විසින් මෙහිදී අවධාරණය කරනුයේ එවැනි සිදුවීම් කීපයක් තිබුණද වැක්සීන භාවිතයෙන් සිදුවන යහපත එහි හානියට වඩා වැඩි බවයි.
මෙයින් එක් දෙයක් පැහැදිලි වේ. එනම් සායනික හෝ සායනික නොවන පරීක්ෂණවලදී මතු නොවූ හානිකර ප්රතිඵල විවෘත සාමාන්ය මහජන භාවිතයේදී මතුවන්නේ නම් එහි අර්ථය අදාළ එන්නත් සඳහා අඩු තරමින් එහි පළමු අදියරේ පරීක්ෂණ මට්ටම්වත් වත් සම්පූර්ණ කර නැති බවය. සාමාන්යයෙන් වැක්සීනයක් නිෂ්පාදනයේදී එහි කෙටිකාලීන සහ දිගු කාලීන අතුරු ආබාධ අධ්යයනය කරමින් එය සුරක්ෂිත සහ කාර්යක්ෂ්ම ලෙස සංවර්ධනය කිරීමට අවම තරමින් වසර 6ක් වත් ගතවන පිළිගත් කරුණකි. එම ක්රියාවලිය අදියර ගණනාවකින් සමන්විතය. බොහෝ වැක්සීන පිළිබඳ පර්යේෂණ සුරක්ෂිතතාව සහ කාර්යක්ෂමතාව පිළිබඳ අපේක්ෂිත ඉලක්කයන්ට ළඟා නොවීම හේතුවෙන් අතරමගදී අත්හැර දමා ඇති වාර අනන්තය. ඖෂධ සතුන්ට ලබාදෙමින් සිදු කරන පර්යේෂණ මට්ටම සාර්ථක වුවහොත් පමණක් එම පර්යේෂණ මිනිසුන්ට අදාලව ඉදිරියට ගෙන යාමට අනුමැතිය ලැබේ. මෙම COVID-19 වැක්සීන සංවර්ධනය කර ඇත්තේ වසරකටත් අඩු කෙටිකලක් තුළය. එවැනි කෙටිකලක් තුළ කෙරෙන පරීක්ෂණ තුලදී අඩු තරමින් කෙටිකාලීන අතුරු ආබාධ හෝ නිසි පරිදි අධීක්ෂණය කරමින්, ගැටළු හඳුනා ගනිමින් ඒවාට නැවත විසඳුම් අත්හදා බලමින් නිවැරදි කිරීමේ ක්රියාදාමය නිසි ලෙස සම්පූර්ණ කළ නොහැකිය. මෙම මතයට එරෙහිව තර්ක කරන ඇතැමුන් පවසන්නේ නව තාක්ෂණය හේතුවෙන් වැක්සීනයක පර්යේෂණ කාලය බොහෝ සෙයින් අඩු කළ හැකි බවය. එසේ වුවද අප විසින් මතක තබාගත යුත්තේ ඖෂධ නිෂ්පාදනයේදී නව තාක්ෂණය යොදාගනිමින් ඒවා ඉක්මණින් නිෂ්පාදනය කළ හැකි වුවත් ස්වාභාවික තත්ත්වයක පසුවන සතුන් හෝ මිනිසුන් වැක්සීනයකට හෝ වෙනත් ඕනෑම ඖෂධයකට දක්වන ප්රතිචාර සම්බන්ධයෙන් ඉක්මන් නිගමනයකට ඒම සඳහා එම සතුන්ගේ හෝ මිනිසුන්ගේ ජීව විද්යාත්මක ක්රියාවලිය ඉක්මන් කරවීමට තාක්ෂණයට නොහැකි බවයි. ඇතැම් අතුරු ආබාධ ක්ෂණිකව මතුවන අතර ඇතැම් ආබාධ වසර ගණනාවකට පසුව මතුවේ. විශේෂයෙන් mRNA වැක්සීන තාක්ෂණය මීට පෙර අත්හදා නොබලන ලද නවතම තාක්ෂණයක් වන අතර එහි අපගේ සෛලවල ජාන වලට දෙන උපදෙස් අඩංගුය. මෙම mRNA කවර නම් අවයව කරා ළඟාවනු ඇත්දැයි යන්න හෝ ඒවායේ දිගුකාලීන ප්රතිඵල කිසිවෙකුත් නොදන්නා බව ඇතැම් විශේෂඥයන් පවසති.
එසේ නම් යුරෝපා ඖෂධ ඒජන්සිය මෙම වැක්සීනවලට මෙතරම් කඩිමුඩියේ අනුමැතිය ලබාදීමට කටයුතු කර ඇත්තේ මන්ද? ඔවුන්ගේ පිළිතුරු ලිපියේ අවසන් කොටසේ මෙසේ සඳහන් වේ.
“..යුරෝපීය සංගමය තුළ, COVID-19 වැක්සීන වෙත ලබා දී ඇත්තේ කොන්දේසි සහිත අලෙවි අනුමැතියකි (CMA). යුරෝපා සංගම් නීතියට අනුව CMA ලබාදෙනුයේ හදිසි මහජන සෞඛ්ය අවශ්යතාවන් පිණිසය. 2020 මාර්තු 20 වැනි දින ලෝක සෞඛ්ය සංවිධානය විසින් වසංගත තත්ත්වයක් ප්රකාශයට පත් කරන ලදි. ලෝකය පුරා පුද්ගලයන්ගේ සෞඛ්යයට සහ සෞඛ්ය ආරක්ෂක පද්ධතීන්ට බරපතල තර්ජනයක් එල්ල කරමින් එම වසංගතය මේ දක්වා පවතී. එය පාලනය කරමින් ඇත්තේ වෛරසය පැතිරීම වැළැක්වීම සඳහා හුදෙක් පුද්ගලයන් ගේ බාහිර සමාජ ආර්ථික ක්රියාකාරිත්වයන් බරපතල හැකිතාක් ලෙස සීමා කිරීම (lockdown) වැනි ඖෂධීය නොවන ක්රියාමාර්ග තුළිනි. ජනගහණය තුළ SARS-CoV-2 වෛරසයට එරෙහිව ප්රතිශක්තිය වර්ධනය වීම පිළිබඳව සාක්ෂි පැවතුණද(ඇතැම් රටවල මෙය 10%ක් පමණ ව.) එය විසින් ප්රති ආසාදනය වැළකීම සිදු නොවේ.
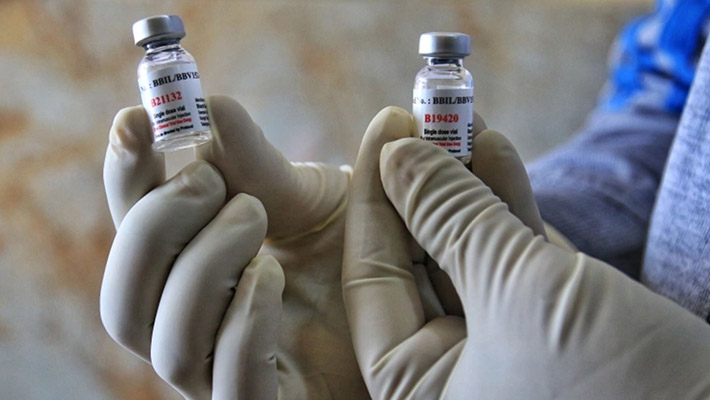
මෙයට අමතරව COVID-19 වසංගතයට ගොදුරුව රෝහල් ගතවූවන් සහ මරණයට පත්වූවන් අති විශාල සංඛ්යාවක් පිළිබඳ වාර්තා ලැබෙමින් පවතී. තවද නව වෛරස් ප්රභේදයන් මතුවෙමින් සෙමින් පැතිරෙමින් පවතී. ඒවායින් සමහරක් වැඩි වේගයකින් පැතිරෙන සුළු අතර වැඩි මාරාන්තික බවකින්ද යුතුය.
මෙම සංදර්භය යටතේ, යුරෝපීය ඖෂධ ඒජන්සිය සතු හදිසි අවශ්යතාවන් සඳහා භාවිතා කළ හැකි උපකරණ අතර වඩාත්ම යෝග්ය යාන්ත්රණය කොන්දේසි සහිත අලෙවි අනුමැතිය වේ (CMA).“
යුරෝපා ඖෂධ ඒජන්සිය තමන් විසින් ලබාදුන් හදිසි අනුමැතිය සාධාරණීකරණයසඳහා ඉදිරිපත් කරන එක් කරුණක් වන්නේ ලෝක සෞඛ්ය සංවිධානය විසින් වසංගත තත්ත්වයක් ප්රකාශයට පත්කිරීමය. ඒ සඳහා ලෝක සෞඛ්ය සංවිධානයේ බලධාරින් විසින් වසංගත තත්ත්වයක් පිළිබඳ ඒ දක්වා පැවැති නිර්වචනය වෙනස් කළ බව සත්යයකි. මෙම COVID-19 වසංගතය සම්බන්ධයෙන් ලෝක සෞඛ්ය සංවිධානයේ චර්යාවන් මුල සිටම ගැටළු සහගතය. ඔවුහු වැක්සීන භාවිතය ප්රවර්ධනය කරනු වස් “Herd Immunity” හෙවත් “සමූහ ප්රතිශක්තිකරණය“ යන්නෙහිද නිර්වචනය පසුගිය වසර තුළ වෙනස් කරන ලද්දේ එම සාමුහික ප්රතිශක්තිකරණයට බලපාන එකම සාධකය වැක්සීන ලෙස එම නිර්වචනයට ඇතුළු කරමිනි. කෙසේවුවද ලෝක සෞඛ්ය සංවිධානය සහ එහි ක්රියාකාරිත්වය වෙනම අධ්යයනය කළ යුතු විෂයයකි.
COVID-19 ආසාදිතයන් හඳුනාගැනීම සඳහා භාවිතාකරන ප්රධානම මෙවලම PCR පරීක්ෂණයයි. එම පරීක්ෂණ ක්රමය සොයා ගනු ලද්දේ Kari Mullis නම් විද්යාඳයා විසිනි. ඒ පිළිබඳව ඔහුට රසායන විද්යාව පිළිබඳ නොබෙල් ත්යාගය පවා හිමිවිය. ඔහු ඒ සම්බන්ධයෙන් පවසා ඇත්තේ මෙම පරීක්ෂණය මගින් පමණක් කිසිවිටෙකත් රෝග නිර්ණය කළ යුතු නොවන බවය. මෙම පරීක්ෂණයේ ඇති අනෙක් ගැටළුව එය ප්රතික්රියා චක්ර 25කට වඩා සිදු කරන්නේ නම් එහි ප්රතිපල සාවද්ය වීමට ඇති ඉඩ 90%කටත් වඩා වැඩි වීමය. දැනට වෙළෙඳපොලේ ඇති සහ ලෝකයේ බොහෝරටවල් භාවිතා කරන ටෙස්ට් කට්ටල මෙම චක්ර ප්රමාණය ඉක්මවා ගිය ඒවා වේ. මේ සම්බන්ධව බොහෝ විශේෂඥයන්ගෙන් මතු වූ විරෝධතා නිසා අවසානයේ ලෝක සෞඛ්ය සංවිධානයට මෙම පරීක්ෂණය භාවිතා කිරීම සම්බන්ධයෙන් උපදෙස් නිකුත් කිරීම සිදු විය. එනම් මෙම පරීක්ෂණය මගින් ආසාදිතයැයි හඳුනාගන්නා ලද පුද්ගලයන් සැබැවින්ම රෝගින්ද යන්න හඳුනාගැනීමට සායනික පරීක්ෂාවක් ද සිදු කළ යුතු බවය. එහෙත් ලෝකයේ බොහෝ රටවල් තම කොරෝනා සංඛ්යා ලේඛනවලට ආසාදිත පුද්ගල සංඛ්යාව ලෙස ඇතුළත් කර ඇත්තේ එම පුද්ගලයන් කිසිදු සායනික පරීක්ෂාවකට ලක්කිරීමෙන් තොරව හුදු PCR පරීක්ෂණ මගින් පමණක් එය තීරණය කිරීමෙනි. එහෙයින් නිසි ලෙස ආරක්ෂාව පිළිබඳව සහතිකයක් දිය නොහැකි වැක්සීන මුදාහැරීම සාධාරණීකරණය සඳහා PCR පරීක්ෂණ මගින් පමණක් ආසාදිතයන් යැයි නම් කරන ලද පුද්ගල සංඛ්යාවන් යොදාගැනීම නිවැරදි නොවේ.
COVID-19 වසංගතය පිළිබඳ ආඛ්යානය පවත්වාගෙන යාමට යොදාගනු ලබන තවත් මෙවලමක් නම් රෝග ලක්ෂණ නොදක්වන නමුත් ආසාදිත පුද්ගලයන් විසින් වෛරසය පතුරුවා හැරීම (asymptomatic transmission) පිළිබඳ ප්රචාරයයි. පර්යේෂණ ගණනාවක් මගින් මෙයට වෙනස් මතයක් තහවුරු කර ඇති නමුත් එම දැනුම කිසිවිටෙකත් භාවිතයට නොයෙදේ.
මරණ සංඛ්යාව සහ රෝහල් පිරී ඉතිරියාම පිළිබඳව සැබෑ තත්ත්වය දැනගනීමට අවශ්ය යමෙකු විසින් කළ යුත්තේ මෙම COVID-19 වසංගතය පැතිර යාමට පෙර වසරවල නිව්මෝනියාව සහ වෙනත් උණරෝග ආදියෙන් මරණයට පත්වූ සංඛ්යාවන් හා COVID-19 වසංගතය පැතිරුණ පසුව ඒ ඒ රටවල සිදු වූ මරණ සංඛ්යාවන් සංසන්දනය කිරීමය.
යුරෝපා ඖෂධ ඒජන්සිය විසින් තමන් මෙම වැක්සීනවලට අනුමැතිය ලබාදීම සඳහා ඉදිරිපත් කරන ඉහත හේතූන් එම ඒජන්සිය විසින් පමණක් භාවිතා කරන ඒවා නොවේ. ලෝකය පුරාම ප්රජා පීඩක ආණ්ඩු මෙම වසංගතය හරහා ජනයාගේ මූලික අයිතීන් යටපත් කිරීම එම තර්කම යොදාගනී. එහෙයින් එම සියලුම ක්ෂේත්රයන් සඳහා පවත්නා සැබෑ තත්ත්වයන් සොයාගැනීමට බරපතල පර්යේෂණයන් අවශ්යව ඇත.
අදාළ වැක්සීන්වලට ඉක්මන් අනුමැතිය සඳහා යුරෝපා බලධාරින් විසින් යුරෝපා ඖෂධ ඒජන්සිය වෙත සිදු කරන ලද බලපෑම් පිළිබඳව පසුගියදා ප්රංශයේ le monde වෙබ් අඩවිය විසින් වාර්තා කර තිබිණි.
මෙයට අමතරව යුරෝපා ඖෂධ ඒජන්සිය විසින් මෙම වැක්සීන සඳහා ලබාදුන් හදිසි අනුමැතිය පිටුපසත් AstraZeneca වැක්සීනය සම්බන්ධව මතුව ඇති ගැටළුකාරි තත්ත්වය යටපත් කරමින් එය භාවිතය අත්හිට වූ රටවලට එය නැවත භාවිතයට උපදෙස් දීම පිටුපසත් එම ඒජන්සියේ විධායක අධ්යක්ෂිකා එමර් කුක් සම්බන්ධයෙන් “ අවශ්යතා පිළිබඳ ගැටුමක් “ ඇතැමුන් මතු කර තිබේ. ඒ ඇය සිය වෘත්තීය ජීවිතයේ සැළකිය යුතු කාලයක් විවිධ ඖෂධ සමාගම් වල අලෙවි ප්රවර්ධන සහ ව්යාපාර කළමණාකරණ කටයුතුවලට සම්බන්ධව සිටි අයෙකු වීම හේතුවෙනි. ඇය 1991 සිට 1998 දක්වා ඇය යුරෝපයේ විශාලතම බහුජාතික ඖෂධ නිෂ්පාදකයන්ගේ සංගමයේ (EFPIA) විද්යාත්මක සහ ඖෂධ පාලක සම්බන්ධතා පිළිබඳ කළමණාකාර තනතුරක් දරමින් එම සංගමය වෙනුවෙන් ලොබි කිරීම්වලට සහභාගි වී ඇත.
රුධිර කැටිගැසීම් හා එමගින් සිදු වූ මරණ සහ රෝගාතුර වීම් හේතුවෙන් යුරෝපයේ රටවල් ගණනාවක් විසින් AstraZeneca වැක්සීනය භාවිතය අත්හිටවූ අවස්ථාවේ ඒ පිළිබඳව සිය පරීක්ෂණ අවසන් වන තෙක් එම තීරණය පවත්වාගෙන යන ලෙස යුරෝපා ඖෂධ ඒජන්සිය විසින් එම රටවලට සහ පොදුවේ සියළු රටවලට උපදෙස් දුන්නේ නම් ලොව පුරා මිනිසුන් සහ ගැහැණුන් සිය ගණනාවක් මරණයට පත් වීම වළකා ගන්නට ඉඩ තිබිණි. එහෙයින් ඒ මරණ පිළිබඳ වගකීම ඒ එජන්සිය සතුය.
එමෙන් ම තවමත් පර්යේෂණාත්මක මට්ටමේ පවතින වැක්සීන මුදාහැර සාමාන්ය මිනිසුන්ට ඒවා භාවිතයට සැලසීම මගින් මිනිස් ජීවිත යොදා ගනිමින් පර්යේෂණ සිදු කිරීමට එය විසින් ඖෂධ සමාගම්වලට ඉඩ හැර තිබේ. මහාචාර්ය සුචරිත් බාක්දි ඇතුළු පිරිස සිය ලිපියේ සඳහන් කර ඇති අන්දමට එය නියුරන්බර්ග් ප්රඥප්තිය උල්ලංඝණය කිරීමකි.
සාමාන්ය ජනතාව මෙම වැක්සීනය ගැනීම ඔවුන් විසින් සියළු කරුණු හා තත්ත්වයන් විමසා බලා ගන්නා ලද නිදහස් තීරණයක් ලෙස සැළකීමට ඇති ඉඩ ඉතා අඩුය. මාධ්යය විසින් දෛනික මරණ සංඛ්යාවන් පිළිබඳ සංඛ්යා ලේඛන හුවා දක්වමින් පවත්වාගෙන යන භීතිකාව, වැක්සීන ගැනීම ප්රතික්ෂේප කළහොත් රැකියා හෝ අනෙකුත් මානව අයිතීන් සහ සිවිල් නිදහස සීමා කිරීම් පිළිබඳ ආණ්ඩු විසින් සෘජුව සහ වක්රව සිදු කරන තර්ජන, වසංගතය හෝ වැක්සීන සම්බන්ධව ආණ්ඩු සහ ඖෂධ සමාගම් විසින් පවත්වාගෙන යන ආඛ්යානය අභියෝග කරන කිසිවක් පළ කිරීම සම්බන්ධ මාධ්ය වාරණ ආදිය ඊට හේතුන්ය.
යුරෝපා ඖෂධ ඒජන්සිය විසින් තම ක්රියාමාර්ග යුක්තිසහගත කිරීමට නිතර ජපකරන මන්ත්රයක් නම් මේ වැක්සීන මගින් යහපත එයින් සිදුවන හානියට වැඩි බවය. යම් අසාධ්ය රෝගීයෙකුගේ ජීවිතය ගලවාගැනීම සඳහා අවදානම් සහගත හෝ පර්යේණාත්මක මට්ටමක පවතින ඖෂධයක් නිර්දේශ කළ හැක්කේ ඔහුගේ හෝ ඇයගේ ජීවිතය ගලවා ගැනීමට වෙනත් කිසිදු විකල්පයක් ඉතුරුව නැති විටෙක පමණි. හානිය සහ යහපත අතර සංසන්දනයක් කළ හැක්කේ එවැනි අවස්ථාවක් සම්බන්ධයෙන් පමණි. නිරෝගී පුද්ගලයෙකුට 99%කට වඩා දිවි ගලවාගැනීමේ ඉඩක් ඇති වසංගතයක් අනාගතයේදී ආසාදනය වීම වැළකීම සඳහා කිසිවෙකුත් නොදන්නා අතුරු ආබාධ සහිත ඇතැම්විට මරණයට පත්විය හැකි තවමත් පර්යේෂණාගාර මට්ටමක පවතින වැක්සීනයක් හෝ වෙනත් ඕනෑම ඖෂධයක් භාවිතයට නිර්දේශ කිරීම ඉහත යහපත සහ හානි පිළිබඳ තර්කයෙන් යුක්ති සහගත කළ හැකි ක්රියාවක් නොවේ.
මෙම වැක්සීන මගින් සිදුවන හානිය එය ගනුලබන ඉතා සුළු පිරිසකට පමණක් බලපාන්නේ නම් (ආණ්ඩු, ඖෂධ සමාගම් සහ මාධ්ය පවසන ආකාරයට මිලියනයක් පමණ දෙනෙකුගෙන් 7 දෙනෙකුට පමණක් හානි සිදු වීමේ ඉඩක් ඇත) වැක්සීන මගින් විපතට පත්වන පිරිසට සහනයක් සහ යුක්තිය ඉල්ලා අධිකරණයට යා නොහැකි ලෙසට සියලු වැක්සීන් සමාගම්වලට ලෝකයේ සියලුම රටවලින් මුක්තියක් ලබා දී ඇත්තේ ඇයි? එවන් අල්ප වූ පිරිසකට කිසියම් වන්දියක් ගෙවීම ඔවුන් වැක්සීන් අලෙවිය මගින් උපයන ඩොලර් හෝ යුරෝ බිලියන සිය ගණනකින් කළ නොහැක්කක්ද? තමන්ට නීතිමය මුක්තියක් ලබා නොදෙන රටවලට වැක්සීන අලෙවි කිරීම ඔවුන් ප්රතික්ෂේප කරන්නේ මන්ද?☐
උපුටා ගැනීම – JDS ( ශ්රී ලංකාවේ ප්රජාතන්ත්රවාදය සදහා මාධ්යවේදියෝ )